应用例(1)氧化态标准样品的测量
作为转换溶出法的测定例,对六胺钌的检测结果进行说明。六胺钌是以氧化态溶解的可逆氧化还原物质,适合作为转换溶出法的标准物质。
图7为测量体系的构成示意图。
对于测量池,将特氟隆烧杯与盐桥连接,盐桥使用装有饱和硝酸钾溶液且管的两端封入多孔玻璃。IDA、Ag / AgCl 参比电极和 Pt 对电极放置在左侧池中用于测量样品,玻璃碳 (GC) 电极作为大电极放置在右侧池中用于沉淀物。参比电极和对电极与恒电位仪的对应端子相连,IDA电极的两个电极端子和GC电极端子通过开关盒与恒电位仪的工作电极端子相连。
该开关盒用于预电解阶段和溶解剥离阶段之间的切换,在预电解阶段,IDA的一个工作电极(生成电极,G电极)连接到恒电位仪,另一个工作电极(收集电极, C电极)连接到大电极。在溶出剥离阶段,构成了一个电路来将大电极连接到恒电位仪。
通过将六胺钌溶解在 pH 4 的标准缓冲溶液中制备样品。用于沉淀的溶液是硝酸银溶解在硝酸钾水溶液(0.1mol/dm 3 )中。用转换溶出法检测六胺钌分以下两个步骤进行。
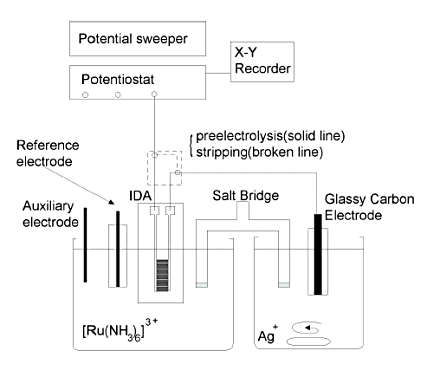
图7-1 转换溶出法的测量池配置
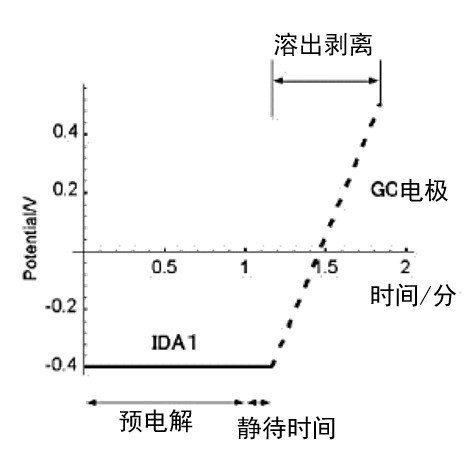
图7-2 转换溶出法的电位印加示意图
如图7-2所示,在第一预电解步骤中,将发生电极的电位设定为比六胺钌的氧化还原电位(图中-0.4V)足够低,继续六胺钌的电解。在此期间,不断搅拌硝酸银溶液。经过预设时间(预电解时间)后,停止搅拌,静置10秒后,立即拨动开关,进行第二阶段的溶出。在溶出剥离过程中,GC 电极电位从 -0.4V 扫描到 0.5V,扫描速率为 20mV/S。此时,将GC电极的电位-电流曲线(转化溶出伏安图)记录在记录仪上。得到的六胺钌的转化溶出伏安图如图1所示。
六胺钌的浓度为1µmol/dm 3。(A)是在-0.4V预电解六胺钌10分钟后获得的银离子的溶出伏安图。另一方面,(b)是在0V下进行10分钟的预电解后得到的。(C) 在无钌六胺溶液中在 -0.4 V 下预电解 10 分钟后得到的。
仅当六胺钌存在下进行电解时,才能观察到大的金属银的溶解剥离峰。在收集电极和发生电极之间插入电流表以监测在预电解阶段流动的电流,并确认在预电解开始后约30秒达到稳定状态。
由上可知,在转换溶解法中,左边电解槽中的六胺钌在发生电极上被还原,生成的还原产物在收集电极上氧化,氧化反应产生的电子用于右边银离子的沉淀池。它变得清晰了。还揭示了在收集器中产生的氧化剂形成了一个自诱导的氧化还原循环,在这个循环中它再次被发生器还原,使得在收集器和GC之间流动的电流达到了一个稳定的状态。
因此,预电解时间与银析出量成正比,说明长期预电解对低浓度检测有效。
六胺钌的浓度为1µmol/dm 3。(A)是在-0.4V预电解六胺钌10分钟后获得的银离子的溶出伏安图。另一方面,(b)是在0V下进行10分钟的预电解后得到的。(C) 在无钌六胺溶液中在 -0.4 V 下预电解 10 分钟后得到的。
仅当六胺钌存在下进行电解时,才能观察到大的金属银的溶解剥离峰。在收集电极和发生电极之间插入电流表以监测在预电解阶段流动的电流,并确认在预电解开始后约30秒达到稳定状态。
由上可知,在转换溶解法中,左边电解槽中的六胺钌在发生电极上被还原,生成的还原产物在收集电极上氧化,氧化反应产生的电子用于右边银离子的沉淀池。它变得清晰了。还揭示了在收集器中产生的氧化剂形成了一个自诱导的氧化还原循环,在这个循环中它再次被发生器还原,使得在收集器和GC之间流动的电流达到了一个稳定的状态。
因此,预电解时间与银析出量成正比,说明长期预电解对低浓度检测有效。
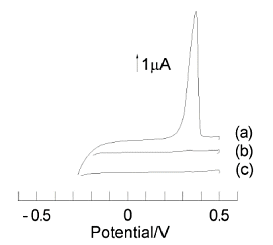
图7-3 1 µ mol/dm3六胺钌转换溶出伏安图
(a),含六胺钌的溶液在 -0.4 V 下预电解 10 分钟。
(b)、将含有六胺钌的溶液在 0 V 下预电解 10 分钟。
(c)不含六胺钌的溶液在-0.4V预电解10分钟。
所有电位扫描速度均为20mV/s
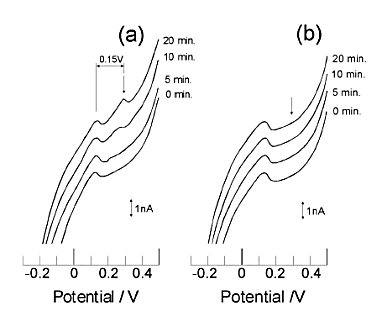
图7-4 10 pmol/dm3六胺钌转换溶出伏安图
(a)用含有六胺钌的溶液测量,(b)不含六胺钌的溶液测量。每个伏安图
右侧的数字是预电解时间。出现在0.3V位置的峰表示检测到六胺钌
图 7-4显示了对10 pmol/dm3的六胺钌应用转化溶出的结果。GC电极的面积、银离子浓度等条件与图7-3不同,以观察更小的溶出峰。(a)是用含有六胺钌的溶液和(b)不含六胺钌的溶液得到的伏安图。在 (a) 中,在 0.3 V 的位置观察到取决于预电解时间的溶出峰,而在 (b) 中,没有观察到相应的峰。图7-5 显示了转换剥离方法的校准曲线[7-2] 。 横轴是六胺钌的浓度,纵轴是在10分钟的预电解时间得到的溶出峰的大小。该检测方法在pmol/dm3区域表现出良好的线性。图中实线为梳状电极的极限电流值[7-3] 与峰宽的计算值,与实验值吻合较好。
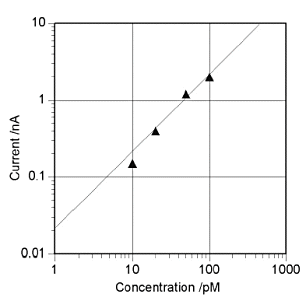
图7-5 pmol/dm3浓度范围的校准曲线,预电解时间为10分钟。实线是计算值。
在转换溶出法中,与通过通常的电化学检测法获得的检测电流相比,可以得到非常大的检测电流。即使在通常的电化学检测方法中使用IDA电极的转换溶出法,也无法检测到10 pmol/dm3的六胺钌,但以计算值评估时,双极模式的极限电流值为0.8 pA[7-1] 。另一方面,通过转换溶出法预电解20分钟得到的峰电流的测量值为0.5nA,这意味着获得了630倍的检测信号。此外,在不能利用氧化还原循环效应的单个电极的情况下,检测电流低至十分之一左右,因而进一步提高了放大效应。
参考文献:
[7-1] J.Janata and A.Bezegh, Anal. Chem., 60, 62R (1988).
[7-2] T. Horiuchi, O. Niwa and H. Tabei, Anal. Chem., 1994, 66, 3500;
[7-3](14) K. Aoki, M. Morita, O. Niwa and H. Tabei, J. Electroanal. Chem., 256(1988) 269.
参考文献:
[7-1] J.Janata and A.Bezegh, Anal. Chem., 60, 62R (1988).
[7-2] T. Horiuchi, O. Niwa and H. Tabei, Anal. Chem., 1994, 66, 3500;
[7-3](14) K. Aoki, M. Morita, O. Niwa and H. Tabei, J. Electroanal. Chem., 256(1988) 269.
